CMC薬事職は薬事分野のスペシャリストです。製剤研究職が専門的な知識を用いて医薬品の価値を最大化するのに対して、CMC薬事職が当局(PMDAなど)が理解できるような書類を作成し、製品の説明をするイメージです。新薬の承認申請から上市後の承認事項の変更対応まで幅広い知識と経験が求められます。本記事では、製薬会社のCMC薬事職について解説します。
CMC薬事職の仕事内容
CMCとはChemistry, Manufacturing and Controlの略で原薬・製剤のChemistry(化学)・ Manufacturing(製造)・Control(品質管理)を指します。具体的には、Chemistryは物性、Manufacturingは製造方法、Controlは分析方法を示しており、原薬と製剤ともに各情報が求められます。CMC薬事とはCMCの分野で薬事申請に向けた戦略や準備、当局対応をおこなう職種です。
CMC薬事の最大の成果物は申請資料(品質パート)の作成です。申請資料の構成は下記のようになっており、CMC薬事は品質パートを担当します。
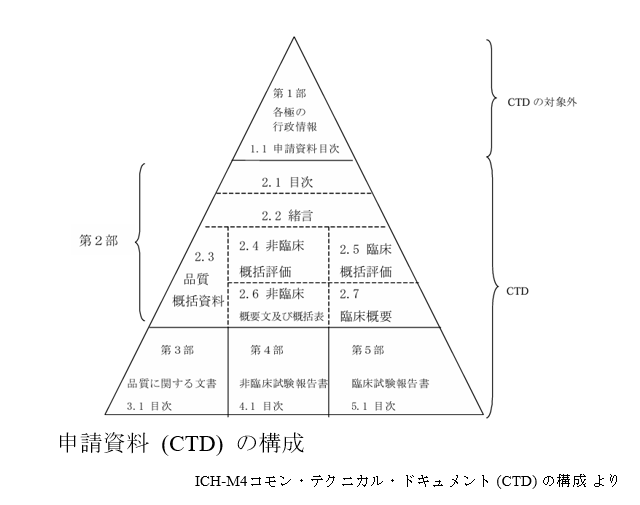
第2部は申請資料の概要とされており、2.3 品質 概括資料は第3部 品質に関する文書の概要です。データ取得は製剤研究職の仕事であるため、データを整理し、当局が求める申請資料の作成をおこないます。
申請資料(品質パート)の内容
第3部 品質に関する文書
3.1 第3部目次
3.2 データ又は報告書
3.2.S 原薬
3.2.S.1 一般情報
3.2.S.2 製造
3.2.S.3 特性
3.2.S.4 原薬の管理
3.2.S.5 標準品又は標準物質
3.2.S.6 容器及び施栓系
3.2.S.7 安定性
3.2.P 製剤
3.2.P.1 製剤及び処方
3.2.P.2 製剤開発の経緯
3.2.P.3 製造
3.2.P.4 添加剤の管理
3.2.P.5 製剤の管理
3.2.P.6 標準品又は標準物質
3.2.P.7 容器及び施栓系
3.2.P.8 安定性
CMC薬事の業務
CMC薬事職の業務としては大きく「新製品の申請対応」と「市販後の変更対応」に分けることができます。
新製品の申請対応
新製品の申請には先ほどのCTDを用意する必要があり、CMC薬事は「2.3 品質概括資料」と「第3部 品質に関する文書」を揃える必要があります。海外からの導入品や海外への導出品を対応することもありますが、規制が国によって若干異なることがあるため、各国のルールに従って資料を準備することが求められます。
- 申請業務の戦略構築や品質管理戦略のとりまとめ
- 申請書類のライティングおよび管理
- 当局との相談、審査対応
市販後の変更対応
医薬品は最終製品の規格だけでなく、原薬の製造場所や規格、製剤の製造方法まで厳密に定められており、それらはすべて承認事項となります。つまり、承認内容と異なる方法で製造することはできません。ただし、上市から年月が経つと、原薬製造所の変更や追加、製造方法の改良が必要になることがあります。その場合は「一部変更承認申請」を行い、承認を得たうえで変更が可能になります。
この取りまとめも、CMC薬事職の業務のひとつです。
- 国内における薬事戦略立案、当局相談、一変申請対応、軽微変更届等の薬事手続きの実施
- 承継や終売を含めたライフサイクルマネジメントにおける薬事対応
CMC薬事職の先輩社員によるインタビュー記事
CMC薬事職で働いている先輩社員のインタビュー記事を紹介します。先輩社員のインタビュー記事を基に実際の業務イメージに役立ててください。
- 塩野義製薬 医薬開発本部薬事部
https://www.shionogi.com/jp/ja/company/journal/20250107.html - 協和キリン 薬事部CMC薬事グループ
https://www.kyowakirin.co.jp/stories/20230714/index.html
CMC薬事職のキャリアパス
初期キャリア:エントリーレベル
製剤や品質管理に関する基本データの整理・文書作成のサポートを行いながら、基礎的な規制要件の習得を目指します。
必要なスキル
- 品質管理・GMPの基礎: 製造プロセスや品質保証の基本概念の理解
- ライティング能力: CTDなどの申請資料の構成や基本的な文書作成スキル
中堅キャリア:スペシャリストレベル
CMC戦略の策定や申請書類の作成・レビューを担い、複数部署との連携でプロジェクトを推進します。
必要なスキル
- 専門知識: 製剤技術、GMP、品質管理、CMCに関する深い知識
- 法規制の理解: PMDA、FDA、EMAなどの規制要件や最新動向の把握
- 申請書類作成力: 複雑なデータや情報を正確にまとめるスキル
シニアキャリア:マネジメント/リーダーポジション
チームを統括し、薬事戦略全体の設計・実行をリードしながら、規制当局や社内外のステークホルダーとの交渉・調整をおこないます。
必要なスキル
- 組織運営・プロジェクト管理: 複数プロジェクトを同時進行で管理できるスキル
- 交渉力・対外交渉能力: 規制当局との折衝や、パートナー企業との調整ができる能力
- 高い英語力: ビジネス会議、文書作成、交渉に対応できるレベル
まとめ
今回はCMC薬事職について解説しました。しかし、新卒からこの職種を採用している会社は多くありません。理由はシンプルで、CMC薬事職の仕事は製造や分析に関する知識が必要になるからです。例えば、下記の資料から製造方法や試験内容をイメージできる必要があります。
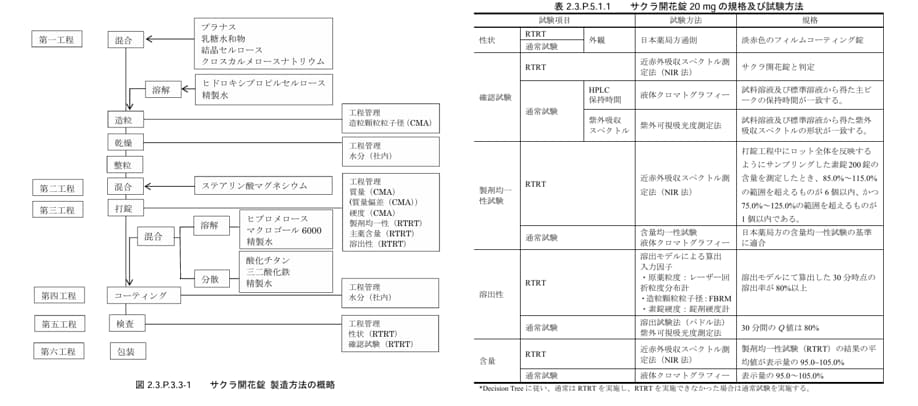
もちろん、ガイドライン通りに資料を作れば業務は進められます。ただし、背景や内容を理解せずに対応すると、矛盾が生じたり、当局と技術者に情報を受け流すだけの担当者となってしまいます。
そのため、多くの会社では、製剤研究、生産技術、品質管理などの経験を積んだうえで、キャリアパスとしてCMC薬事職に進むケースが一般的です。
もし新卒でCMC薬事職を目指す場合、入社後に実務を学ぶ機会を積極的に作ることをおすすめします。工場の立会いや見学、セミナーなどを活用して、知識を広げていきましょう。また、面接でも経験をカバーする熱意があることをしっかりアピールしましょう。
